በካርቦን አሲድ እና በቢካርቦኔት መካከል ያለው ቁልፍ ልዩነት ካርቦን አሲድ ገለልተኛ የኬሚካል ውህድ ሲሆን ባዮካርቦኔት ግን አሉታዊ ኃይል ያለው የኬሚካል ውህድ ነው።
ካርቦኒክ አሲድ ካርቦን ዳይኦክሳይድ በውሃ ውስጥ ሲቀልጥ በመፍትሔው ውስጥ የሚፈጠር ደካማ አሲድ ሲሆን በኬሚካል ፎርሙላ H2CO3። ባዮካርቦኔት የሚፈጠረው በሶስት ኦክሲጅን አቶሞች፣ በሃይድሮጂን አቶም እና በካርቦን አቶም ከኬሚካል ፎርሙላ HCO3-. ጋር በማጣመር ነው።
ካርቦኒክ አሲድ ምንድነው?
ካርቦኒክ አሲድ H2CO3 ነው። አንዳንድ ጊዜ ይህንን ስም የምንሰጠው ካርቦን ዳይኦክሳይድ በውሃ ወይም በካርቦን የተሞላ ውሃ ውስጥ እንዲሟሟላቸው ነው።ይህ የሆነበት ምክንያት ካርቦናዊ ውሃ አነስተኛ መጠን ያለው H2CO3 ስላለው ነው። በተጨማሪም ካርቦን አሲድ ደካማ አሲድ ነው, እና እንደ ካርቦኔት እና ባይካርቦኔት ሁለት ዓይነት ጨዎችን መፍጠር ይችላል. የዚህ ውህድ ሞላር ክብደት 62.024 ግ/ሞል ነው።
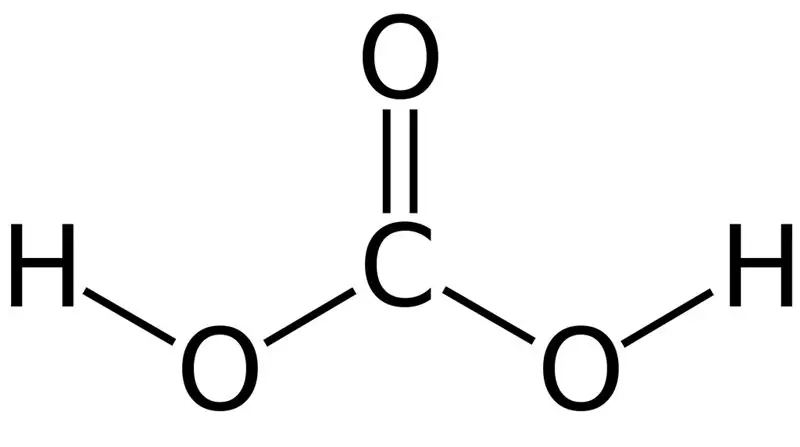
ምስል 01፡ የካርቦኒክ አሲድ ኬሚካዊ መዋቅር
ካርቦን ዳይኦክሳይድ በውሃ ውስጥ ሲቀልጥ በካርቦን ዳይኦክሳይድ እና በካርቦን ዳይኦክሳይድ መካከል ባለው ሚዛን ውስጥ ይገባል። ሚዛኑ እንደሚከተለው ነው፡
CO2 + H2O ⟷ H2CO3
የተትረፈረፈ ካርቦን አሲድ ወደ ቤዝ ከጨመርን ቢካርቦኔት ይሰጣል። ነገር ግን ፣ ከመጠን በላይ የመሠረት መጠን ካለ ፣ ከዚያ ካርቦን አሲድ ካርቦናዊ ጨዎችን ይሰጣል። በትክክል ፣ ካርቦን አሲድ ከካርቦን ካርቦን ጋር የተቆራኙ ሁለት የሃይድሮክሳይል ቡድን ምትክ ያለው የካርቦሊክ አሲድ ውህድ ነው።ከዚህም በላይ ፕሮቶን የመለገስ ችሎታ ያለው ፖሊፕሮቲክ አሲድ ነው. ሁለት ተንቀሳቃሽ ፕሮቶኖች አሉት፣ስለዚህ እሱ በተለይ ዳይፕሮቲክ ነው።
Bicarbonate ምንድን ነው?
ቢካርቦኔት የሚፈጠረው በሶስት ኦክሲጅን አተሞች፣ በሃይድሮጂን አቶም እና በካርቦን አቶም ጥምረት ነው። የዚህ ጥምረት ምርት ion ወይም ከፕሮቶኖች የበለጠ ኤሌክትሮኖች ያሉት ውህድ ሊሆን ይችላል። የኬሚካል ፎርሙላ HCO3–. ያለው እንደ ኬሚካላዊ ዝርያ ልንገልጸው እንችላለን
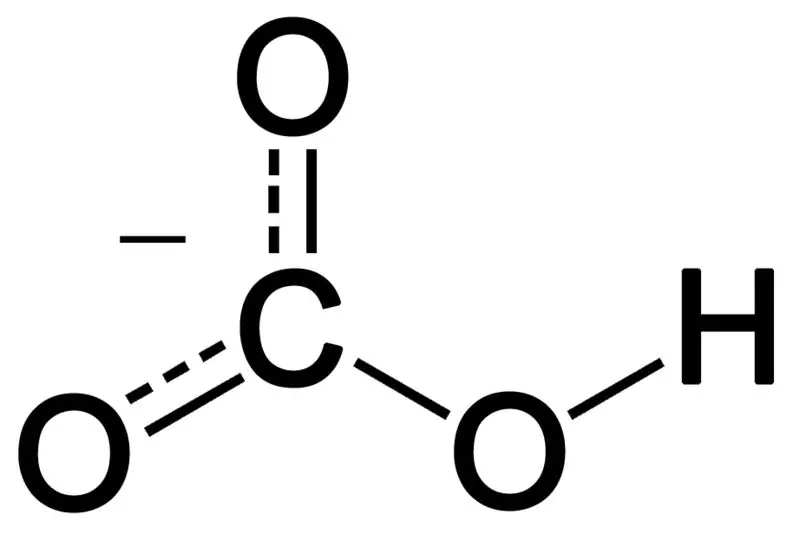
ምስል 02፡ የባይካርቦኔት አኒዮን ኬሚካላዊ መዋቅር
ይህ ውህድ የሰውነታችን ፒኤች ማቋቋሚያ ስርዓት ወሳኝ አካል ነው፣በተለምዶ አነጋገር፡ የአንድን ሰው ደም አሲዳማ ባልሆነ ወይም መሰረታዊ ባልሆነ ሁኔታ ውስጥ የመቆየት ሃላፊነት አለበት። በተጨማሪም, ሆዱ ምግቡን ማብላቱን ካጠናቀቀ በኋላ የምግብ መፍጫውን ጭማቂ ለመጠበቅ እንደ መንገድ ያገለግላል.በተጨማሪም በዝናብ ውሃ ውስጥ የሚገኘው ካርቦን አሲድ ድንጋይ ሲመታ የባዮካርቦኔት ionዎችን ይፈጥራል። ይህ የባይካርቦኔት ion ፍሰት የካርበን ዑደቱን ጠብቆ ለማቆየት አስፈላጊ ነው።
በካርቦን አሲድ እና በቢካርቦኔት መካከል ያለው ልዩነት ምንድነው?
ካርቦኒክ አሲድ ካርቦን ዳይኦክሳይድ በውሃ ውስጥ ሲቀልጥ በመፍትሔ ውስጥ የሚፈጠር ደካማ አሲድ ሲሆን የኬሚካል ቀመሩም H2CO3 ነው። ቢካርቦኔት የሚፈጠረው በሶስት ኦክሲጅን አቶሞች፣ በሃይድሮጂን አቶም እና በካርቦን አቶም ከኬሚካል ፎርሙላ HCO3- ጋር በማጣመር ነው። በካርቦን አሲድ እና በቢካርቦኔት መካከል ያለው ቁልፍ ልዩነት ካርቦን አሲድ ገለልተኛ የኬሚካል ውህድ ነው, ነገር ግን ባይካርቦኔት አሉታዊ የኬሚካል ውህድ ነው. ከዚህም በላይ ካርቦን አሲድ አረፋን ፣ ፊዚ መጠጦችን ፣ የቆዳ በሽታዎችን ለማከም ፣ በአፍ ውስጥ መታጠብ ፣ ወዘተ. ፣ ቢካርቦኔት ግን እንደ መጋገር (እንደ እርሾ ወኪል) ያሉ የምግብ ዝግጅቶችን ይጠቀማል እና የፒኤች ለውጦችን የመቋቋም ችሎታ ይሰጣል ።
የሚከተለው ኢንፎግራፊክ በካርቦን አሲድ እና በቢካርቦኔት መካከል ያለውን ልዩነት በሠንጠረዥ መልክ ለጎን ለጎን ለማነፃፀር ያጠቃልላል።
ማጠቃለያ - ካርቦኒክ አሲድ vs ቢካርቦኔት
ካርቦኒክ አሲድ H2CO3 ነው። ባዮካርቦኔት በሶስት ኦክሲጅን አቶሞች፣ በሃይድሮጂን አቶም እና በካርቦን አቶም በኬሚካላዊ ቀመር HCO3- ጥምረት ይመሰረታል። በካርቦን አሲድ እና በቢካርቦኔት መካከል ያለው ቁልፍ ልዩነት ካርቦን አሲድ ገለልተኛ የኬሚካል ውህድ ነው ፣ ቢካርቦኔት ግን አሉታዊ ኃይል ያለው የኬሚካል ውህድ ነው።







